Elemente võib klassifitseerida kumbagi metallid või mittemetallid nende omaduste põhjal. Enamasti võite öelda, et element on metall, lihtsalt vaadates selle metallilist läiget, kuid see pole ainus erinevus nende kahe elementide üldise rühma vahel.
Metallid
Enamik elemente on metallid. Siia kuuluvad leelismetallid, leelismuldmetallid, siirdemetallid, lantaniidid ja aktiniidid. Sisse perioodilisustabel, metallid eraldatakse mittemetallidest siksakjoonega, liikudes läbi süsiniku, fosfori, seleeni, joodi ja radooni. Need ja neist paremal asuvad elemendid on mittemetallid. Elemente, mis asuvad otse joonest vasakul, võib nimetada metalloidid või semimetallid ning nende omadused peavad olema metallide ja mittemetallide omaduste vahel. Nende eristamiseks võib kasutada metallide ja mittemetallide füüsikalisi ja keemilisi omadusi.
Metalli füüsikalised omadused:
- Läikiv (läikiv)
- Hea küll dirigendid soojus ja elekter
- Kõrge sulamistemperatuur
- Suur tihedus (suuruse järgi raske)
- Tempermalmist (saab vasardada)
- Kõrgtugev (saab tõmmata juhtmetesse)
- Tavaliselt soliidne kell toatemperatuuril (erandiks on elavhõbe)
- Läbipaistmatu õhukese lehena (ei näe läbi metallide)
- Metallid on helilised või annavad löömisel kellukese heli
Metalli keemilised omadused:
- Iga metalli aatomi väliskeses on 1-3 elektroni ja kaotavad elektronid hõlpsalt
- Korrodeerub kergesti (nt oksüdeerumisega kahjustatud, näiteks tuhm või rooste)
- Kaotada elektrone lihtsalt
- Moodustavad aluselised oksiidid
- Fave madalam elektronegatiivsus
- On head redutseerivad ained
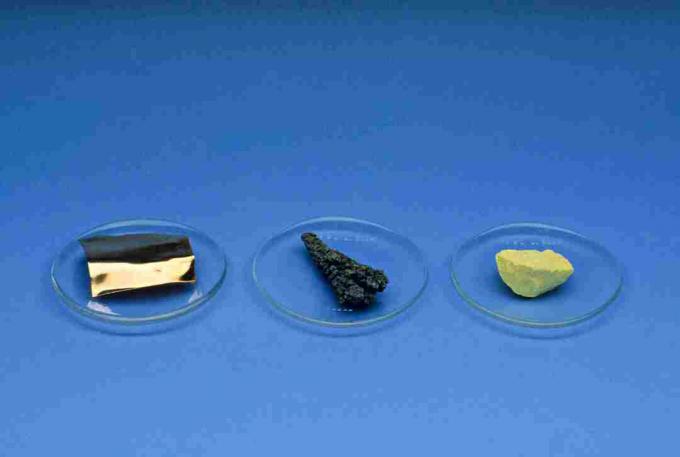
Mittemetallid
Mittemetallid, välja arvatud vesinik, asuvad perioodilise tabeli paremal küljel. Mittemetallideks on vesinik, süsinik, lämmastik, fosfor, hapnik, väävel, seleen, kõik halogeenid ja väärisgaasid.
Mittemetallilised füüsikalised omadused:
- Pole läikiv (tuhm välimus)
- Kehvad soojus- ja elektrijuhid
- Mittelugevad tahked ained
- Haprad kuivained
- Toatemperatuuril võivad olla tahked ained, vedelikud või gaasid
- Läbipaistev õhukese lehena
- Mittemetallid pole helilised
Mittemetallilised keemilised omadused:
- Tavaliselt on nende väliskeses 4-8 elektroni
- Valentselektrone saab hõlpsasti omandada või jagada
- Moodustavad happelisi oksiide
- On kõrgemad elektronegatiivsused
- On head oksüdeerivad ained
Nii metallidel kui ka mittemetallidel on erinevad vormid (allotrobid), millel on erinev välimus ja omadused. Näiteks grafiit ja teemant on mittemetallilise süsiniku kaks allotropi, ferriit ja austeniit on kaks raua allotropi. Kui mittemetallidel võib olla metotüüp, siis näevad kõik metallide allüünlad välja sellised, mida me arvame metallina (läikivad, läikivad).